 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
当弱酸(HA)和弱酸盐组成的缓冲溶液组分浓度比为下述关系时,缓冲容量最大的是()。
A.HA:A-=1:9
B.HA:A-=9:1
C.HA:A-=1:2
D.HA:A-=1:1
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.HA:A-=1:9
B.HA:A-=9:1
C.HA:A-=1:2
D.HA:A-=1:1
 答案
答案
 更多“当弱酸(HA)和弱酸盐组成的缓冲溶液组分浓度比为下述关系时,缓冲容量最大的是()。 A、HA:A-=1:”相关的问题
更多“当弱酸(HA)和弱酸盐组成的缓冲溶液组分浓度比为下述关系时,缓冲容量最大的是()。 A、HA:A-=1:”相关的问题
第1题
由一元弱酸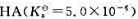 和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
第2题
A.弱共辄酸碱对(包括弱酸―弱碱盐,弱碱―弱酸盐共辄酸碱对)
B.强共辄酸碱对(包括强酸-强碱盐,强碱-强酸盐共辄酸碱对)
C.弱共辄酸碱对(包括弱酸―弱酸盐,弱碱-弱碱盐共辄酸碱对)
D.强共辄酸碱对(包括强酸―强酸盐,强碱―强碱盐共辄酸碱对)
第3题
A.醋酸pKa=4、74
B.甲酸pKa=3、74
C.一氯乙酸pKa=2、86
D.二氯乙酸pKa=1、30
E.三氯乙酸pKa=、0、64
F.苯酚pKa=9、95
第4题
某弱酸HA总浓度为2.0×10-4mol/L。于λ520nm处,用1cm比色皿测定,在不同pH值的缓冲溶液中,测得吸光度值如下:
| pH | 0.88 | 1.17 | 2.99 | 3.41 | 3.95 | 4.89 | 5.50 |
| A | 0.890 | 0.890 | 0.692 | 0.552 | 0.385 | 0.260 | 0.260 |
求:
第5题
准确量取30.00ml弱酸,加水稀释至100ml。以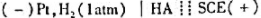 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
第6题
第7题
A.浓的强酸和稀的强碱溶液反应
B.浓的强碱和稀的强酸溶液反应
C.稀的强碱和浓的弱酸反应
D.生成了一种强碱弱酸盐
第8题
缓冲溶液的pH值决定于()。
A.此缓冲溶液的缓冲容量
B.组成此缓冲溶液的弱酸或弱碱的KA.Kb
C.共轭酸碱对的浓度比值的大小
D.此缓冲溶液的缓冲范围