 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列关于平衡常数K的说法中,正确的是()
A.平衡常数K只与反应本身及温度有关
B.改变反应物浓度或生成物浓度都会改变平衡常数K
C.加入催化剂可以改变平衡常数K
D.在任何条件下,化学平衡常数是一个恒定值
 答案
答案
A、平衡常数K只与反应本身及温度有关
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.平衡常数K只与反应本身及温度有关
B.改变反应物浓度或生成物浓度都会改变平衡常数K
C.加入催化剂可以改变平衡常数K
D.在任何条件下,化学平衡常数是一个恒定值
 答案
答案
A、平衡常数K只与反应本身及温度有关
 更多“下列关于平衡常数K的说法中,正确的是()”相关的问题
更多“下列关于平衡常数K的说法中,正确的是()”相关的问题
第1题
A.K越大,达到平衡时,反应进行的程度越大
B.K越小,达到平衡时,反应物的转化率越大
C.K随反应物浓度的改变而改变
D.K随温度和压强的改变而改变
第2题
A.在平衡常数表达式中,反应物浓度用起始浓度表示,生成物浓度用平衡浓度表示
B.可逆反应中,反应物的转化率增大,一定导致化学平衡常数增大
C.可以用化学平衡常数来定量描述化学反应的限度
D.平衡常数的大小与温度、浓度、压强、催化剂有关
第6题
A.围绕同一星球运行的行星或卫星,k值不相等
B.不同星球的行星或卫星,k值均相等
C.公式只适用于围绕太阳运行的行星
D.以上说法均错
第7题
A.增加SO2的浓度,正反应速率先增大,后保持不变
B.增加SO2的浓度,正反应速率逐渐增大
C.增加SO2的浓度,平衡常数增大
D.增加SO2的浓度,平衡常数不变
第8题
过度排放CO2会造成”温室效应“,科学家正在研究如何将CO2转化为可以利用的资源,其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为: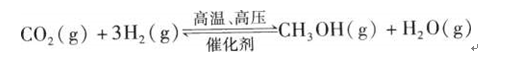
请填空:
问题一、写出上述反应的平衡常数表达式K=()。
问题二、在容积为2L的密闭容器中,用一定量二氧化碳与一定量氢气在一定条件下合成甲醇,实验结果如下图。以下说法正确的选项是()。
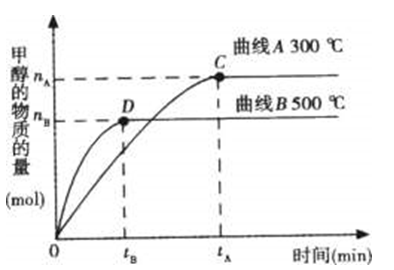
A在300℃,从反应开始到平衡,甲醇的平均反应速率
B反应体系从300℃升温到500℃,平衡常数K变大
C该反应的正反应为放热反应
D处于C点的反应体系从300℃升温到500℃n(H2)/n(CH3OH)增大
问题三、25℃、1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为()。
问题四、选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极应加入或通入的物质是,正极的电极反应式为()。
第9题
A.热力学温标的零度是-273.15 ℃,叫作绝对零度
B.随着科学技术的发展,获得绝对零度的低温是可能的
C.热力学温标的每1 K大小和摄氏温标的每1 ℃大小相同
D.在国际单位制中,温度的单位是 ℃
第10题
A.筛分设备的k应取1.25
B.筛分作业若在原煤仓前,且用准轨受煤坑受煤,k应取值不大于1.5
C.筛分作业若在原煤仓前,k应根据受煤设施的种类考虑取值
D.筛分作业若在原煤仓后,k应取值1.15
第11题
A.越省力的机械,其机械效率越高
B.做的有用功越多,机械效率就越高[来源:学,科,网Z,X,X,K]
C.做的总功越少,机械效率就越高
D.额外功在总功中占的比例越小,机械效率越高