 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在高温下CO2按下式分解2CO2(g)→2CO(g)+O2(g),在压力为101.325kPa下,CO2的解离度在1000K和1400K时分别为
已知在高温下CO2按下式分解2CO2(g)→2CO(g)+O2(g),在压力为101.325kPa下,CO2的解离度在1000K和1400K时分别为2.50×10-5和1.27×10-2。若在1000K到1400K的温度区间内
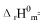 及1000K时的
及1000K时的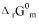 和
和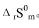 。
。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在高温下CO2按下式分解2CO2(g)→2CO(g)+O2(g),在压力为101.325kPa下,CO2的解离度在1000K和1400K时分别为2.50×10-5和1.27×10-2。若在1000K到1400K的温度区间内
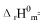 及1000K时的
及1000K时的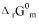 和
和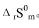 。
。
 答案
答案
 更多“已知在高温下CO2按下式分解2CO2(g)→2CO(g)+O2(g),在压力为101.325kPa下,CO2的解离度在1000K和1400K时分别为”相关的问题
更多“已知在高温下CO2按下式分解2CO2(g)→2CO(g)+O2(g),在压力为101.325kPa下,CO2的解离度在1000K和1400K时分别为”相关的问题
第1题
2CO2(g)+6H2(g)=CH3CH2OH(g)+3H2O(g)
请利用你的热力学知识说明此反应.
已知: 2CO2(g)+6H2(g)=CH3CH2OH(g)+3H2O(g)
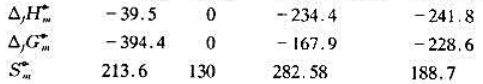
你认为为了提高反应转化率,合成条件应有什么改变?试提出你的看法.
第2题
在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
问题一、已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol2C(s)+O2(g)=2CO(g)△H=-221.0kJ/molC(s)+O2(g)=CO2(g)△H=-393.5kJ/mol尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=()
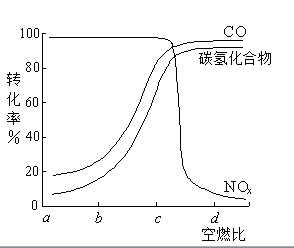
问题二、某研究性学习小组在技术人员的指导下,按以下流程探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。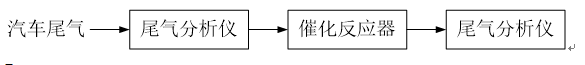
①实验过程中除空燃比不同外,其他条件:汽车尾气的流速、()等必须相同。
②在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为()时,催化剂对汽车尾气的催化效果最好。
问题三、CO分析仪以燃料电池为工作原理,其装置如下图,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。以下说法错误的选项是()。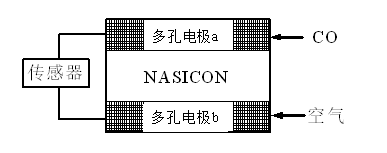
A负极的电极反应式为:CO+O2—―2e-=CO2
B工作时电极b作正极,O2-由电极a流向电极b
C工作时电子由电极a通过传感器流向电极b
D传感器中通过的电流越大,尾气中CO的含量越高
第3题
硝基乙酸在酸性溶液中的分解反应
(NO2)CH2COOH(1)→CH3NO2(I)+CO2(g)
为一级反应.25℃,101.3kPa下,测定不同反应时间产生的CO2(g)体积如下:
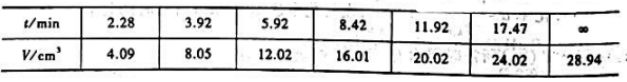
反应不是从t=0开始的.求速率常数k.
第4题
关于尿素合成的说法正确的是()。
A.CO与NH3在气相中反应,所以应在高温下反应
B.CO2与NH3在气相中反应,所以应在高温下反应
C.甲铵高温下易分解,反应在液相中进行,所以应在高压低温下反应
D.反应在液相中进行,温度应低于甲铵分解温度,压力应高于甲铵饱和蒸汽压
第5题
298.15KO2(g),CO2,H2O(1)的 分别为205.03J·K-1·mol-1,213.6J·K-1·mol-1,69.91J·K-1·mol-1,反应CH3COOH(1)+2O2(g)→2CO2(g)+2H2O(1)的
分别为205.03J·K-1·mol-1,213.6J·K-1·mol-1,69.91J·K-1·mol-1,反应CH3COOH(1)+2O2(g)→2CO2(g)+2H2O(1)的 =3.04J·K-1·mol-1),则298.15 K时,CH3COOH(1)的
=3.04J·K-1·mol-1),则298.15 K时,CH3COOH(1)的 ______
______
第6题
A.2v(NH3) = v(CO2)
B.密闭容器中混合气体的密度不变
C.密闭容器中混合气体的平均摩尔质量不变
D.密闭容器中氨气的体积分数不变
第7题
化学计量关系
溴代异丁烷与乙醇钠在乙醇溶液中按下式进行反应:
i-C4H9Br+C2H5ONa→NaBr+i-C4H9OC2H5
(A) (B) (P) (S)
已知反应物的初始浓度分别为cA0=50.5mol/m3和cB0=76.2mol/m3,原料中无产物存在。在95℃下反应一段时间后,分析得知cB=37.6mol/m3,试确定此时其余组分的浓度。
第8题
A.升高温度可使该反应的正反应速率增大,逆反应速率减小
B.增大压强,可以使 NO 和 CO 完全转为为无污染的 N2 和 CO2,而消除污染
C.该反应反应物总能量小于生成物总能量
D.使用高效催化剂可降低反应的活化能,反应速率增大
第9题
A.通CO的一极是电池的正极
B.负极发生的电极反应是O2+2CO2+4e-=2CO32-
C.负极发生的电极反应是CO+CO32--2e-=2CO2
D.正极发生氧化反应
第10题
A.Q1+Q2+Q3
B.0.5Q1-0.5Q2+1.5Q3
C.0.5(Q1+Q2+Q3)
D.0.5Q1-1.5Q2+0.5Q3
第11题
已知CaCO3(s)=CaO(s)+CO2(g)的Kc(1500 K)=0.50,在此温度下CO2又有部分分解成CO,即CO2=CO+
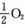 。若将1.00 mol CaCO3装入1.00 dm3真空容器中,加热到1500 K达平衡时,气体混合物中O2的摩尔分数为0.15。计算容器中CaO的物质的量n(CaO)。
。若将1.00 mol CaCO3装入1.00 dm3真空容器中,加热到1500 K达平衡时,气体混合物中O2的摩尔分数为0.15。计算容器中CaO的物质的量n(CaO)。