 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[判断题]
向已达平衡的反应N2O4(g)2NO2(g)中加入Ar并保持体系的体积不变,则反应向左移动。()
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“向已达平衡的反应N2O4(g)2NO2(g)中加入Ar并保持体系的体积不变,则反应向左移动。()”相关的问题
更多“向已达平衡的反应N2O4(g)2NO2(g)中加入Ar并保持体系的体积不变,则反应向左移动。()”相关的问题
第1题
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的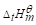
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.
第2题
2NO2(g).25℃下该反应的初始速率实验数据如表3-1:

(1)写出反应速率方程;
(2)计算25℃时反应速度系数k;
(3)co(NO)=0.0030mol·L-2,co(O2)=0.0015rmol·L-2时,相应的初始速半为多少?
第3题
2
(g)达到平衡.此时,向反应系统中加入一定量的惰性组分H2O(g),则标准平衡常数Kθ(),C6H5C2H5(g)的平衡转化率α(),C6H5C2H3(g)的摩尔分数y(C6H5C2H3)().(选择填入:增大、减小、不变.)
第5题
当下述反应2SO2kg)+O2(g)=2SO3(g)达到平衡后,在反应系统中加入一定量的惰性气体,对于平衡系统有何影响?试就加入惰性气体后系统的体积保持不变或总压力保持不变这两种情况加以讨论。
第6题
nB=nB/nC=1,则此反应的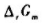 =();
=();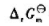 =();Kθ=().
=();Kθ=().
第8题
水蒸气通过灼热的C(石墨)发生下列反应:
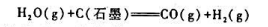
此平衡系统的组分数C=(),相数P=(),自由度F=().这说明生成的CO(g),H2(g)在气相中的摩尔分数与()有关.
第9题
A.向左进行
B.向右进行
C.处于平衡状态
D.无法确定
第11题
已知反应 的
的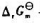 与T的关系为
与T的关系为
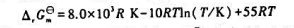
则此反应的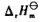 与T之间的函数关系为
与T之间的函数关系为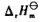 =();
=();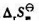 与T之间的函数关系为
与T之间的函数关系为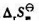 =();InKθ与T之间的函数关系为lnKθ=().若T=1000K,p=200kPa,则题给反应的标准平衡常数Kθ和B2(g)的平衡转化率α分别为Kθ=(),α=().
=();InKθ与T之间的函数关系为lnKθ=().若T=1000K,p=200kPa,则题给反应的标准平衡常数Kθ和B2(g)的平衡转化率α分别为Kθ=(),α=().