 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应C(s)+H2O(g)=CO(g)+H2(g)在一密闭容器中进行。下列说法或结论正确的是()。
A.当v(CO)(正)=v(H2)(正),时,反应达到平衡状态
B.其他条件不变,适当增加C(s)的质量会使平衡正向移动
C.保持容器体积不变,充入少量He使体系压强增大,反应速率一定增大
D.其他条件不变,仅将容器的体积缩小一半,再次达到平衡时,H20(g)的平衡浓度可能是原来的2.1倍
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.当v(CO)(正)=v(H2)(正),时,反应达到平衡状态
B.其他条件不变,适当增加C(s)的质量会使平衡正向移动
C.保持容器体积不变,充入少量He使体系压强增大,反应速率一定增大
D.其他条件不变,仅将容器的体积缩小一半,再次达到平衡时,H20(g)的平衡浓度可能是原来的2.1倍
 答案
答案
 更多“反应C(s)+H2O(g)=CO(g)+H2(g)在一密闭容器中进行。下列说法或结论正确的是()。”相关的问题
更多“反应C(s)+H2O(g)=CO(g)+H2(g)在一密闭容器中进行。下列说法或结论正确的是()。”相关的问题
第2题
下述3个反应:①S(s)+O2(g)→SO2(g)
②H2(g)+O2(g)→H2O2(l)
③C(s)+H2O(g)→CO(g)+H2(g)
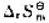 由小到大的顺序为()。
由小到大的顺序为()。
第4题
已知 CO2(g) NH3(g) H2O(g) CO(NH2)2(s)


通过计算说明,反应CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s)
(1)在298K时,反应能否正向自发进行?
(2)在1000K时,反应能否正向自发进行?
第5题
试用热力学数据表计算823K下以下反应的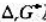 及
及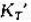 :
:
(1)CoO(s)+H2(g)=Co(s)+H2O(g)
(2)CoO(s)+CO(g)=Co(s)+CO2(g)
并讨论H2和CO还原CoO为Co的可能性,你以为哪种方法更好一些?为什么?
第6题
A.升高温度,可加快反应速率
B.将块状固体粉碎,可加快反应速率
C.平衡时,反应停止了
D.平衡时,CO的浓度不再改变
第7题
A.生成1molCO的同时生成1molH2
B.容器中物质的总质量不发生变化
C.n(H2O):n(H2)=1 :1
D.v逆(H2O)=v正(CO)
第8题
A.增加焦炭的量
B.保持体积不变,充入H2O气使体系的压强增大
C.将容器的体积增大一倍
D.将容器的体积缩小为一半
第9题
已知数据(298.15K)(如表5-2所示)。
表5-2 | |||||
物质 | C(石墨) | H2(g) | N2(g) | O2(g) | CO(NH2)2(s) |
S_{m}^{Theta }/(Jcdot mol^{-1}cdot K^{-1}) | 5.740 | 130.68 | 191.6 | 205.14 | 104.6 |
Delta _{c}H_{m}^{Theta }/(kJcdot mol^{-1}) | -393.51 | -285.83 | 0 | 0 | -631.66 |
物质 | NH3(g) | CO2(g) | H2O(g) |
Delta _{f}G_{m}^{Theta }/(kJcdot mol^{-1}) | -16.5 | -394.36 | -228.57 |
求:298.15K下,CO(NH2)2(s)的标准摩尔生成吉布斯函数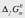 ,以及反应CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s)的KΘ。
,以及反应CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s)的KΘ。
第10题
A.34.04kPa
B.43.54kPa
C.56.66kPa
D.156.0kPa